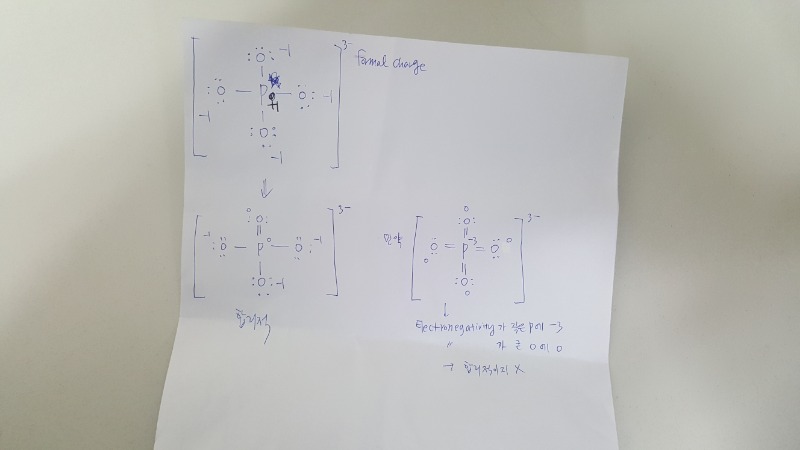
P의 formal charge가 +3 이 나올수 있는 구조는 절대 나올 수 없습니다 P가 central atom이고 valence가 5개이므로 학생이 말씀하신것 처럼 모두 double bond로 하면 4개의 O의 formal charge는 0이 될 수 있겠지만 P는 -3의 formal charge를 갖게됩니다 처음에 P와 O를 모두 single bond로 하면 4개의 O는 모두 -1의 formal charge를 가지며 P는 +1의 formal charge를 가집니다 이 때 산소 1개의 lone pair가 P와 double bond를 형성하는 것이 formal charge 관점에서 최선이 되는 구조입니다
또한 앞서 말한바와 같이 P의 form charge는 +1보다 클 수 없습니다 4개의 결합이 있는데 +3이 나올 수는 없지요
학생이 그린 구조가 정확히 무엇인지는 모르겠으나 혹시 오른쪽 아래 그림이라면 형식전하가 +3이 될 수 없습니다
3-2의 문제는 학생의 말씀이 맞습니다 수업내용도 그러합니다. 하지만 문제에 따라서 단순히 이렇게 물어보고 값을 구하라고 한다면 외부압력과 물의 증기압만으로 문제를 해결해달라는 의미가 될 수 있습니다 물론 엄밀히 말하면 학생의 말처럼 조건을 제시해주어야 하는 것이 맞습니다 이런 문제를 문장으로 학생이 말씀하신 내용을 포함하여 설명이 옳은지 물어볼 수 있습니다 그러므로 학생이 생각하시는 것이 옳은것으로 더 정확하지만 이 문제는 단순하게 해석해서 값을 구하시면 됩니다
개념은 ap로 빨리 하셔도 문제풀이는 SAT강의를 들으셔야 합니다 문제 유형이 다르고 AP에서 다루지 않는 colligative property가 SAT에는 나오며 비록 SAT가 문제 수준이 낮아도 문제 풀이 연습은 반드시 해야 합니다
답변이 도움이 되었기를 바랍니다
